近日,先进能源科学与技术广东省实验室(简称“东江实验室”)新能源和新型储能研究中心与兰州大学化学化工学院、中国科学院近代物理研究所(简称“近代物理所”)重离子科学与技术全国重点实验室材料研究中心合作,在手性分离膜研究方面取得重要突破。研究团队依托兰州重离子加速器,结合创新的电压驱动原位组装策略,成功制备出一种具有同手性特征的氢键生物杂化框架核孔膜(HBF@PET),实现了对氨基酸对映体的高效、精准分离。相关成果发表在国际化学期刊《美国化学会志》(Journal of the American Chemical Society)上。
手性结构在生命过程和药物活性中扮演着关键角色,获得高纯度的单一对映体化合物对于医药、农业等领域具有重要意义。然而,传统手性分离技术通常存在能耗高、效率低等问题,现有手性膜材料也常因结构不稳定、活性位点分布不均,难以兼顾高选择性和高通量。
结构基石:核孔膜提供理想平台
本研究的核心基石,在于团队在重离子辐照制备核孔膜领域的深厚积累。核孔膜具有孔道垂直贯通、尺寸可调特性,是后续功能材料得以精准组装的前提。
研究团队利用兰州重离子加速器提供的高能Xe离子束,对聚对苯二甲酸乙二醇酯(PET)薄膜进行均匀辐照,随后通过精确控制的径迹蚀刻工艺,成功制备出孔道结构高度规整、孔径均一(约400纳米)的纳米通道膜。这种核孔膜不仅提供了机械强度,其孔道内壁光滑、贯通性好的特点,更为后续功能材料的均匀负载提供了理想的限域空间和结构基础。
精准组装:电压驱动赋予手性识别能力
在获得高质量核孔膜这一精密骨架后,如何为其装上能识别手性分子的功能单元是另一大挑战。为此,研究团队创新性地引入电压驱动的原位组装策略。在2伏直流电压驱动下,带负电的牛血清白蛋白(BSA)和有机配体分子(HTBAPy)通过电泳作用高效进入PET核孔膜的纳米通道内并实现均匀分布。BSA与配体通过定向氢键共组装,形成氢键生物杂化框架(HBF)。该结构既保留了BSA的天然手性微环境,又获得氢键有机框架的结构稳定性。分析结果表明,HBF沿通道内壁形成连续晶态层,使通道孔径缩小至约1.5纳米,与氨基酸分子尺寸相当,显著增强了膜材料的手性识别能力。
性能与前景:稳定高效,为手性药物分离开辟新路径
实验结果显示,该HBF@PET核孔膜对色氨酸、精氨酸等多种氨基酸对映体均表现出优异的识别性能。尤其在对组氨酸的分离中,L-His在BSA手性口袋中能与更多残基形成氢键,而D-His仅与两个残基形成氢键。更强的结合作用阻碍了L-His的扩散,D-His则因弱相互作用快速通过通道,从而实现高效分离。该膜在9个循环(12小时/循环)或连续120小时运行后,D-His通量仍保持初始值的80%以上;在pH 2~11溶液中浸泡24小时后结构稳定,无材料泄漏,展现出优异的化学与机械稳定性。
本研究充分发挥兰州大学在先进化学合成领域的技术积淀,以及近代物理所与东江实验室在核孔膜制备方面的平台优势,通过将可控核孔膜与生物功能材料有机结合,有效解决了手性膜稳定性与选择性难以兼顾的关键难题,为开发新型生物杂化分离膜、实现手性药物绿色分离提供了新思路。
论文第一作者为博士生常新月和宋艳霞,通讯作者为兰州大学汪宝堆教授和东江实验室、近代物理所段敬来研究员。研究工作得到了国家自然科学基金和甘肃省科技领军人才计划等项目的资助。
论文链接:https://pubs.acs.org/doi/10.1021/jacs.5c22150
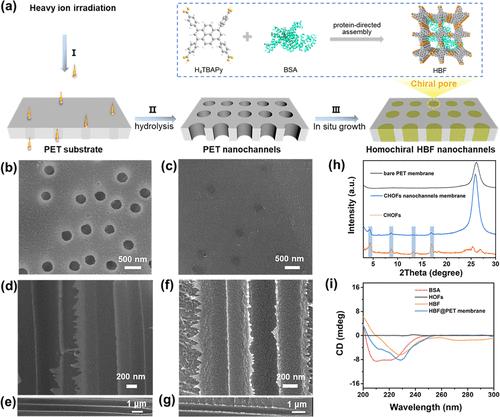
图:手性分离新型核孔膜制备与表征
